镁科研:镁合金骨愈合机制的研究进展
发布日期:2023-07-17 浏览次数:2139
当下的研究为镁合金在骨科领域的应用提供了理论基础和见解。然而,镁合金促进骨愈合的机制非常复杂,涉及到多种不同的细胞类型、众多的调节因子、相互交织的信号网络以及多步骤的平衡调控。目前还有很多生物学作用和机制未得到充分研究和证实,尤其是关于不同细胞对碱性环境和H2响应的具体机制仍不明确。此外,现有的研究主要集中于验证已知的成骨因子和通路在镁合金促进骨愈合过程中的参与程度,对镁合金促进骨愈合的机制缺乏全面系统和创新性的阐释。
同时,为了更好地模拟体内生物效应,我们还需要研究细胞之间的相互作用,特别是对两种或两种以上细胞之间的串扰进行深入研究。此外,大部分细胞研究都以优化设计和体内植入为最终目标,我们迫切需要直接探索和验证镁合金体内植入所引起的生物效应和潜在机制。
深入了解镁合金骨愈合机制将为优化设计提供更多理论依据,并促进其在骨再生治疗中的应用。因此,我们需要进一步扩大研究范围,全面而系统地解析镁合金在骨科领域中促进骨愈合的机制,特别是关于细胞间相互作用以及镁合金体内植入所引发的生物效应方面的研究是十分必要的。只有这样,我们才能更好地利用镁合金材料,并推动其在骨再生治疗中的应用取得更大的突破。
镁及合金因其优异的力学性能、生物可降解性和生物活性在骨科植入物领域备受关注,其促进骨修复的能力已被证实。在骨修复过程中,调控宿主组织和植入物之间的生物相互作用是植入成功的关键,镁合金对宿主细胞功能状态的调节及对种植部位微环境的塑造值得关注和研究。全面阐明镁合金植入后与宿主的相互作用及其机制,将为镁合金设计的优化提供更多的理论依据,促进镁合金在骨再生治疗中的应用。遗憾的是,当前镁合金在骨再生过程中对宿主细胞功能的全面调控及其潜在机制仍未完全阐明。
最近,中国医科大学附属第一医院的郭澍教授、中国医科大学口腔医学院的王强研究员以及中科院金属研究所的谭丽丽研究员等人对镁合金在骨修复机制方面的研究进展进行了综述。他们系统地总结了镁合金降解产生的不同浓度镁离子、碱性环境以及氢气释放对相关骨愈合细胞的影响,并详细阐述了镁合金在免疫调控、血管再生、成骨和破骨细胞功能调控方面的作用及其潜在机制。此外,他们还为进一步探索镁合金在骨修复机制方面提供了方向和建议。这项综述为我们深入了解镁合金在骨修复中的作用机制提供了重要的参考和指导。
对于骨愈合的成功,良好的免疫微环境调控、血运重建和骨重塑是非常关键的。在骨愈合的过程中,炎症、修复和重塑是连续而部分重叠的三个阶段。不同谱系的细胞,包括免疫细胞、成血管相关细胞、成骨细胞、骨细胞和破骨细胞等,依次参与其中。镁合金能够以不同的方式与这些细胞相互作用,从而实现对骨愈合的全面调控。图1展示了这种相互作用的概述。因此,这篇综述从免疫调控、血管再生、成骨和破骨细胞功能调控四个方面系统地总结了镁合金在骨愈合机制中的作用。通过深入了解这些机制,我们可以更好地理解镁合金在骨修复中的作用,并为进一步的研究和临床应用提供方向和指导。
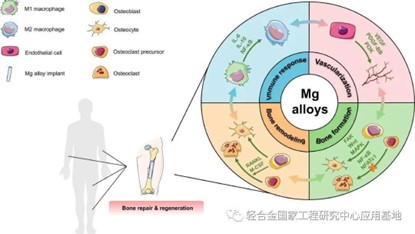
图1 镁合金作为骨植入物通过参与免疫调节、血管再生、成骨和破骨细胞功能调节从而促进骨愈合的示意图
镁合金在免疫反应中,特别是巨噬细胞的极化行为上具有双向调控的作用。在植入早期,镁合金参与了一系列炎症活化过程,包括蛋白吸附、炎症细胞募集、单核细胞分化、巨噬细胞M1表型极化和吞噬作用等。当镁合金降解稳定后,适当释放的镁离子、氢氧根和氢气可以促进巨噬细胞向M2表型极化转变,从而创造出有利于组织再生的抑炎免疫微环境。在这个过程中,TRPM7/PI3K/AKT1s、TLR-4/MYD88/NF-κB等信号通路的活化起到了关键作用。在良好的免疫微环境塑造下,M2型巨噬细胞与间充质干细胞等骨愈合相关细胞相互作用,促进骨再生,并参与缺损部位的血管再生过程。图2展示了镁合金通过调控巨噬细胞极化来塑造骨愈合微环境的作用及其潜在机制。通过了解这些调控机制,我们可以更好地利用镁合金来促进骨愈合,并为临床应用提供更多的可能性。
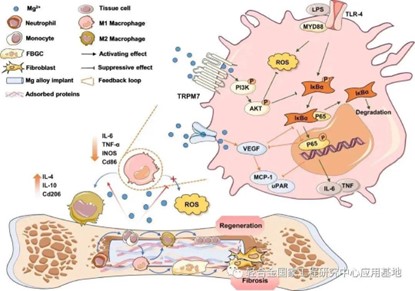
图2 镁合金通过调控巨噬细胞极化塑造骨愈合微环境的示意图
除此之外,镁合金还参与了血管再生的全过程,包括低氧诱导因子(HIF)、血管内皮生长因子(VEGF)等血管再生相关因子的产生、血管基底膜的降解、内皮细胞的增殖、迁移、管形成以及血管成熟和稳定等步骤。如图3所示。需要特别注意的是,感觉神经及其分泌的降钙素基因相关肽(CGRP)在镁离子促进内皮细胞迁移和管形成过程中发挥着重要的作用。CGRP通过激活CGRP-FAK-VEGF信号轴参与骨缺损部位的血管再生。此外,在适当浓度的镁离子作用下,血管生成关键因子血小板衍生生长因子-BB(PDGF-BB)的上调可以实现血管和骨的相互连接,从而显著促进骨愈合的进行。这些发现为利用镁合金来促进骨愈合提供了新的机制和途径。
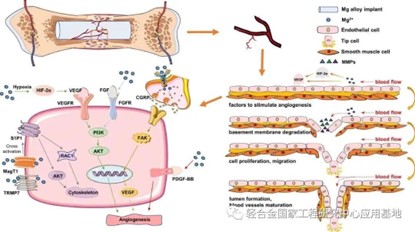
图3 镁合金降解产生的镁离子促进骨愈合过程中血管再生的示意图
镁合金对成骨相关细胞和破骨细胞具有双重调控作用,这是更为重要的。研究表明,镁合金降解产生的不同浓度的镁离子、碱性环境和pH值对成骨相关细胞和破骨细胞有不同的影响。表1展示了不同浓度镁离子对不同成骨相关细胞的成骨分化能力的影响。实验证明,镁合金降解产生的镁离子和碱性环境通过激活或抑制复杂的信号通路网络来调节成骨相关细胞和破骨细胞的生物行为,如图4和图5所示。特别值得一提的是,除了一般的成骨相关通路的激活外,镁离子还可以通过镁离子膜转运蛋白TRPM7和MagT1介导的通路来促进成骨分化的发生。
表1 不同浓度镁离子对不同成骨相关细胞成骨分化能力的影响
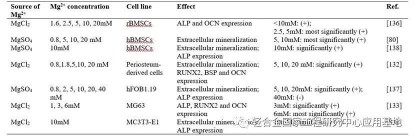
图4 镁合金促成骨作用相关信号通路示意图

图5 镁抑制破骨细胞分化和功能的分子机制示意图
实际上,镁合金在骨科领域的应用研究还处于早期阶段,仍然存在许多未解决的问题和挑战。
目前的研究确实为镁合金在骨愈合方面的应用提供了一些理论基础和初步见解。这些研究显示,镁合金具有良好的生物相容性,并且其降解产物对骨组织有促进作用。此外,镁合金还可以调节细胞的增殖、分化和分泌活动,从而促进骨细胞的生长和骨组织的再生。
然而,镁合金促进骨愈合的机制还不完全清楚,需要进一步深入研究。尤其是在镁合金与骨细胞及其他相关细胞之间的相互作用机制方面,我们仍然知之甚少。此外,镁合金的降解过程对骨细胞和骨组织的影响也需要详细研究。
为了更好地应用镁合金于骨科治疗,我们需要进一步探索镁合金的材料特性、优化设计和制备工艺,以提高其生物相容性和力学性能。此外,临床试验和长期随访研究也是必要的,以评估镁合金在骨愈合中的实际疗效和安全性。
总的来说,虽然目前的研究为镁合金在骨科领域的应用提供了初步的理论基础,但仍需进一步深入研究和验证其具体的促进骨愈合机制,同时优化设计和临床实践的探索也是非常重要的。
免责声明:本网站所转载的文字、图片与视频资料版权归原创作者所有,如果涉及侵权,请第一时间联系本网删除。




















